H5亚型流感病毒是发现最广泛的禽流感病毒,已在世界各地的家禽和野生鸟类中造成多次疾病暴发。H5病毒在自然界长期传播后,通过积累突变和与其他流感病毒亚型重组经历了广泛的进化。
在我国日常家禽监测中,从2021年9月至2022年3月在中国收集的26767个野生鸟类和家禽样本中分离出13个H5N1病毒,表明H5N1病毒也曾传入中国。
虽然携带2.3.4.4b HA基因支系的H5N1病毒在不同大陆均有广泛的检测,但在不同国家检测到的毒株的遗传关系在很大程度上是未知的,其生物学特性也很少被评价。

H5N1病毒引发禽流感爆发
相关数据显示,2020年1月至2022年3月期间,携带2.3.4.4 HA基因支系的不同H5高致病性禽流感病毒共发生了7778起疫情,其中H5N1病毒引起暴发4284起,H5N2病毒引起62起,H5N3病毒引起15起,H5N4病毒引起14起,H5N5病毒引起158起,H5N6病毒引起24起,H5N8病毒引起3221起。H5N2和H5N6病毒的暴发主要发生在亚洲,H5N3和H5N4病毒的暴发仅在欧洲有报道,H5N5病毒在欧洲和亚洲均有暴发。在欧洲、非洲、亚洲和北美的一些国家都报告了H5N1病毒引起的疫情。
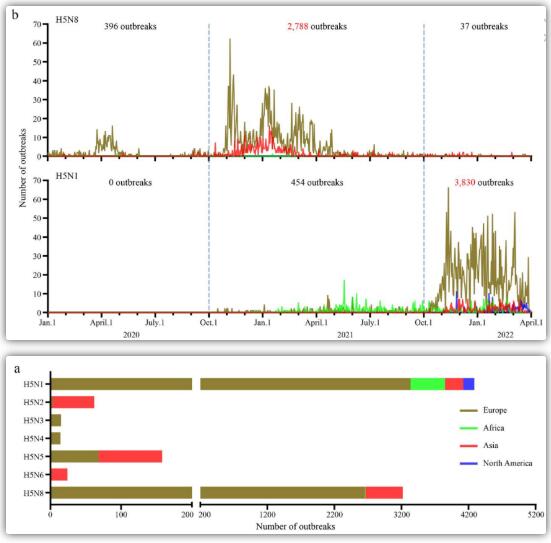
中国分离的H5N1流行特点
在我国积极监测禽流感病毒期间,从2021年9月至2022年3月收集的26767个样本中共分离出811个禽流感病毒。这些病毒属于9种不同的HA亚型。99个H5病毒中有13个被确认为H5N1亚型。序列分析表明,H5N1病毒均携带HA基因2.3.4.4b支。从死亡野鸭的肺组织中分离到1株病毒,从活禽市场收集的鸡、鸭、鹅和鸽子拭子中分离到12株病毒。
H5N1病毒的系统发育分析
为了解中国H5N1病毒的来源及与其他国家H5N1病毒的遗传关系,研究人员对13株H5N1病毒进行了全基因组测序,并下载了其他国家报道的220株H5N1代表性毒株的基因组序列进行系统发育和基因型分析。
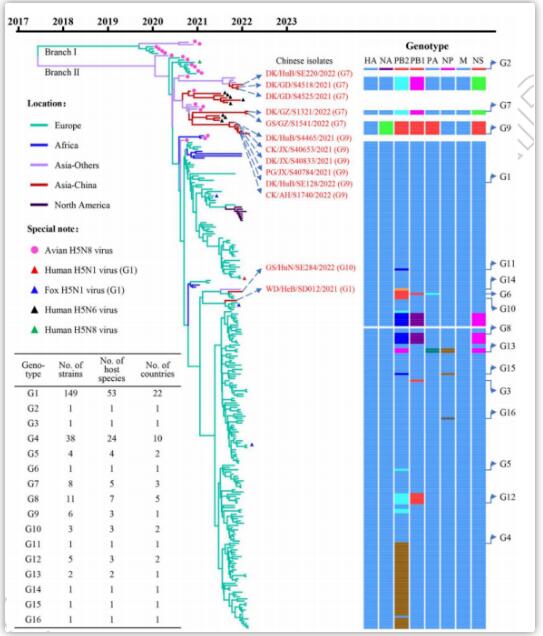
这些结果表明,H5N1病毒的NA和内部基因具有明显的多样性,根据基因组差异,在欧洲、非洲、亚洲和北美检测到的233株H5N1病毒形成了16种不同的基因型。
H5N1病毒的时空传播特点
为了进一步了解病毒在各基因型中的出现、基因星座和时空分布,研究人员分析了各病毒基因型检测的时间和地点。结果发现G1病毒于2020年10月首先出现在欧洲,尤其是荷兰,并在欧洲国家流行到2022年2月。2021年11月在中国检测到G1病毒,随后2022年1月在非洲检测到了G1病毒,北美于2021年12月至2022年2月之间也检测到了G1病毒。
研究人员发现G1病毒是在欧洲、非洲、亚洲、北美等22个国家的野鸟或家禽中发现的传播最广的毒株。

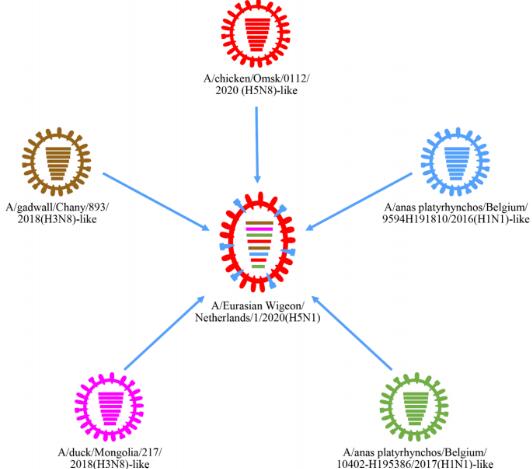
H5N1病毒在小鼠体内的复制和毒力
为了评价H5N1病毒在哺乳动物中的复制和毒力,研究人员对中国在小鼠中发现的8个代表性毒株进行了检测,包括1个G1病毒、3个G7病毒、3个G9病毒和1个G10病毒。
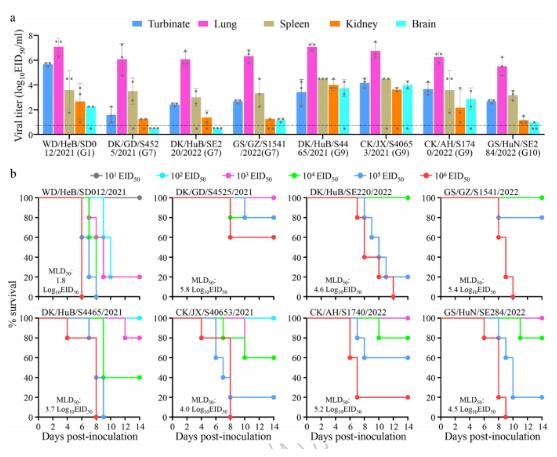
上述结果表明,中国检测到的H5N1病毒在小鼠体内具有不同的致病型,G1病毒WD/HeB/SD012/2021在小鼠体内的毒性最强。
H5N1病毒的疫苗现状
疫苗接种是中国控制高致病性禽流感的主要策略,研究人员开发了不同的疫苗毒株,以防止不同进化支或亚进化支的病毒感染。
H5- re11疫苗种子病毒是针对携带2.3.4.4h HA支的H5病毒研制的,于2018年12月至2021年12月用于疫苗生产。H5- re13和H5- re14是最近更新的疫苗种子病毒,分别针对新检测到的携带HA枝2.3.4.4h和HA枝2.3.4.4b基因的H5病毒开发的,自2022年1月以来已用于疫苗生产。
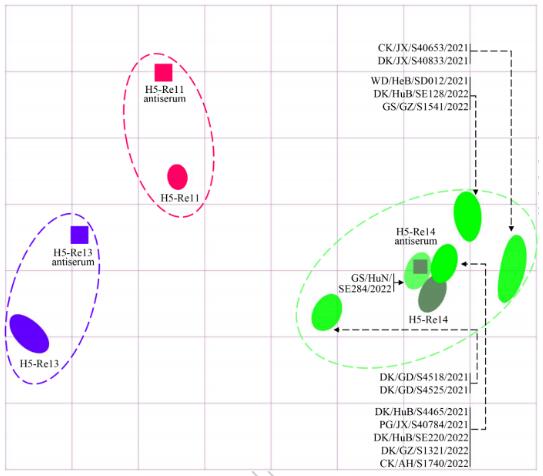
H5N1病毒对全球家禽业造成了严重破坏,为控制这一疾病已消灭了7 000多万只家禽。值得注意的是,仅在美国就有大约3000万只家禽被宰杀。该研究证明我国研制的H5- re14种子病毒对携带2.3.4.4b HA枝的H5病毒具有保护作用,此外,先前已有研究表明,新型H5/H7三价疫苗对携带2.3.4.4b HA枝的H5N1、H5N6和H5N8病毒均具有可靠的保护作用。
鉴于H5N1病毒在野生鸟类中广泛传播,这些病毒极有可能继续危害家禽业,并对人类公共卫生构成威胁。因此,研究人员强烈建议高风险国家为其家禽接种疫苗,以保护它们免受高致病性H5禽流感的侵袭。

